Explicamos o que é o ácido acético, como é sua fórmula e as propriedades que apresenta. Além disso, suas características, usos e exemplos.


O que é ácido acético?
Ácido acético, ácido metilcarboxílico ou também ácido etanóico é chamado um composto orgânico que pode ser encontrado como o íon acetato ou etanoato ([C2H3O2]–). Está presente no vinagre, líquido ao qual confere o cheiro característico e o sabor azedo.
É um ácido fraco resultado usual em certos processos de fermentação, como as que ocorrem no vinho ou na fruta. É amplamente utilizado em aplicações de química orgânica e em vários processos industriais.
Sua massiva produção no mundo se deve ao fato de ser um composto útil na obtenção de outras substâncias orgânicascomo o ácido acrílico.
Veja também: ácido sulfúrico
fórmula de ácido acético
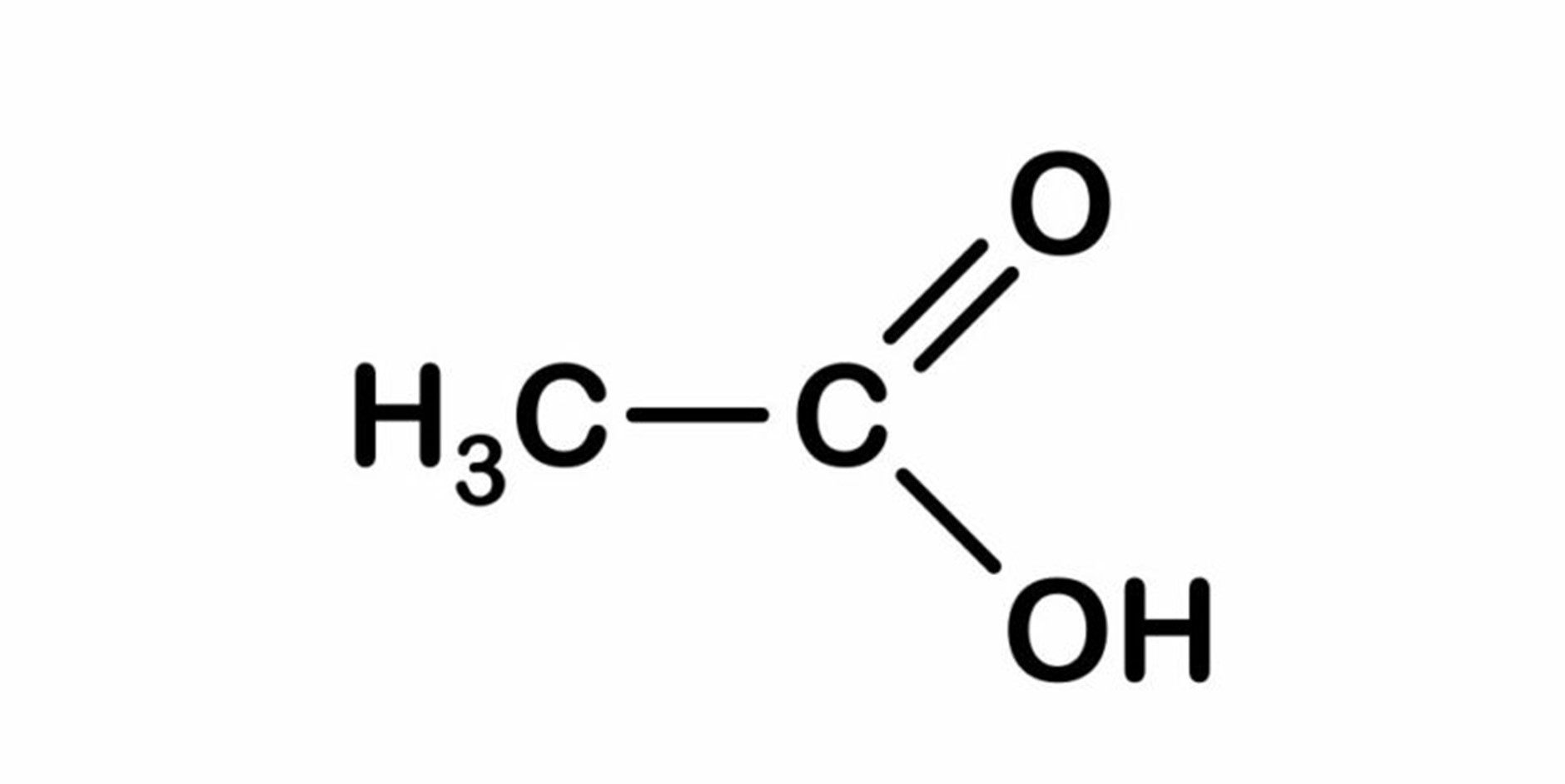
ácido acético tem a fórmula química C2H4O2 e a fórmula semidesenvolvida CH3COOH. Daí resulta que é um grupo metila (CH3-) ligado por uma ligação simples de um átomo de carbono a um grupo carboxila (-COOH).

Solubilidade do ácido acético


O ácido acético é uma substância bastante polar porque possui um grupo polar (-COOH), embora também tenha algumas características apolares devido ao seu grupo (-CH3). Devido à presença de ambos os grupos em sua estrutura, é uma substância que é solúvel em água (solvente polar)mas também é solúvel em muitas substâncias orgânicas menos polares.
Peso molecular do ácido acético
- Peso molecular. O ácido acético tem um peso molecular de 60,05 g/mol.
- Densidade. A densidade do ácido acético é 1049 kg/m3.
- Aparência. Pode ser um líquido claro com forte odor de vinagre e sabor ácido, ou um sólido incolor na forma de pequenos cristais regulares.
vinagre e ácido acético


O vinagre contém 3% a 5% de ácido acético dissolvido em água, juntamente com pequenas quantidades de ácido tartárico (C4H6O6) e ácido cítrico (C6H8O7).
Foi descoberto pela primeira vez na produção de vinho, uma vez que os barris mal guardados para onde vazava ar e oxigênio sofreram o processo de fermentação das bactérias Mycoderma aceti, que converte álcool etílico em vinagre. Dizia-se então que o vinho era “picante”.
O vinagre, no entanto, constitui uma parte importante da gastronomia humana e é produzido a partir de diferentes fontes: maçãs, uvas ou álcoois artificiais.
É essencial no preparo de marinadas, ceviche, picles ou como molho para saladas. Também usado na conservação de alimentos porque retarda os processos de decomposição da matéria orgânica.
Propriedades do ácido acético
O ácido acético é um ácido bastante fracoapesar de ser inflamável e corrosivo ao mesmo tempo, além de ser uma substância higroscópica (que absorve a água da umidade do ambiente).
Em altas concentrações pode, portanto, irritar a pele, olhos ou membranas mucosas, tanto por inalação quanto por deglutição. É um ácido frequentemente secretado pelos seres vivos, como metabólito e substrato para as enzimas acetiltransferases.
Seu ponto de ebulição é de 118 °C, enquanto seu ponto de fusão é de 17 °C.
Ácido acético glacial


O ácido acético glacial é chamado resultado do congelamento do ácido acético, em que a água que faz parte do composto forma cristais facilmente removíveis do composto. Uma vez que os cristais de água tenham sido separados dos cristais de ácido acético, o ácido retorna ao estado líquido.
Assim, quando falamos de ácido acético glacial, nos referimos a ácido acético anidroou seja, sem água.
Perigo de ácido acético
Em termos gerais, o ácido acético com o qual há contato no vinagre e outras soluções É encontrado em concentrações tão baixas que não é perigoso. em absoluto.
Porém, em altas concentrações, é um ácido irritante Capaz de causar queimaduras na pele, danos permanentes aos olhos e irritação das membranas mucosas.
Não é um composto particularmente inflamávelmas em soluções a mais de 25%, seus gases podem ser igualmente corrosivos e perigosos para a vida humana e animal, por isso é manuseado em exaustor de fumaça.
Obtenção de ácido acético
Algumas das principais formas de obtenção do ácido acético são através das seguintes reações:
- carbonilação do metanol. Reação entre metanol e monóxido de carbono que resulta em ácido acético.
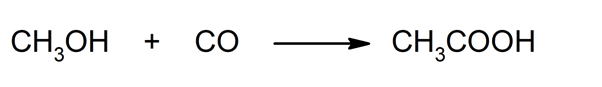
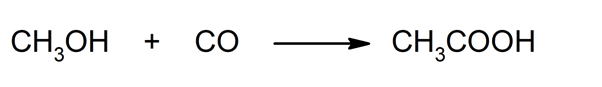
- oxidação de etileno. O etileno é oxidado usando um metal como catalisador, paládio (Pd) neste caso.


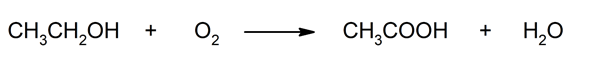
- fermentação oxidativa. Na presença de oxigênio, bactérias do gênero Acetobacter Eles podem produzir ácido acético a partir de certos compostos alcoólicos.

Aplicações de ácido acético


O ácido acético tem inúmeras aplicações em diferentes indústrias humanas, tais como:
- É utilizado como aditivo no controle da traça da cera (doença chamada galeriose) na apicultura.
- É um componente importante (formando sais ou ésteres) para fazer nylon, raiom, celofane e outros filmes sintéticos.
- É utilizado na fixação de substâncias para preservação de tecidos orgânicos em laboratórios (como formol).
- É usado em produtos químicos para revelação fotográfica.
- É usado como corante para revelar lesões do vírus do papiloma humano (HPV) na medicina.
- É um componente comum de produtos de limpeza comerciais e removedores de manchas.
- Tem muitos usos culinários como o vinagre: para lavar legumes, como molho, etc.
Pode te ajudar: Ácido clorídrico