Explicamos o que é o ácido sulfúrico, como é sua fórmula e as propriedades que possui. Além disso, quais são suas características e usos.


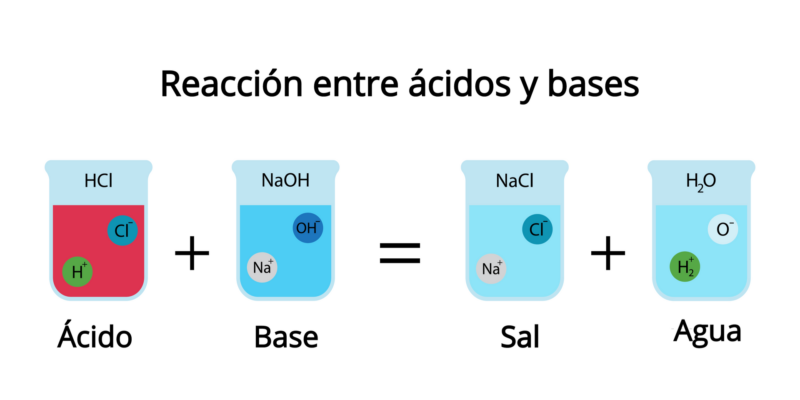
O que é ácido sulfúrico?
ácido sulfúrico é chamado um composto químico altamente corrosivo. É um dos produtos químicos mais gerados e utilizados no mundo, dadas as suas inúmeras aplicações na indústria e na síntese de outros insumos químicos.
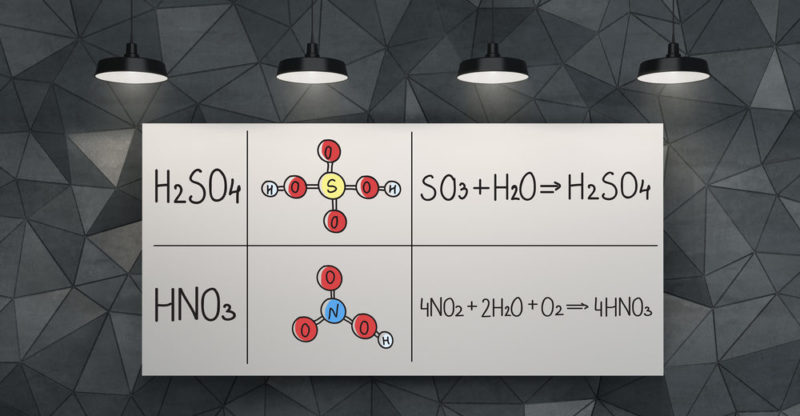
É conhecido como ácido tetraoxossulfúrico (VI) ou tetraoxossulfato de hidrogênio (VI). E é formado por um átomo de enxofre, dois de hidrogênio e quatro de oxigênio. É representado pelo fórmula molecular H2TÃO4.
Veja também: ácido clorídrico
História do ácido sulfúrico

O ácido sulfúrico foi observado pela primeira vez na Idade Média muçulmana, quando os alquimistas o obtinham de cristais de sais de sulfatomaterial que conheciam como vitríolo, do latim vítreo (“cristal”). Por esta razão, o ácido sulfúrico era tradicionalmente chamado de óleo de vitríolo, licor de vitríolo ou espírito de vitríolo.
De acordo com esta tradição, o vitríolo era considerado o produto químico mais importante do mundo, por isso poderia ser usado como pedra filosofal (substância que deveria ser capaz de converter metais em ouro ou prata). Por esta razão, várias substâncias foram chamadas de vitríolo azul ou romano (sulfato de cobre II, CuSO4), vitríolo branco (sulfato de zinco, ZnSO4), vitríolo verde (sulfato de ferro II, FeSO4), vitríolo vermelho (sulfato de cobalto II, CoSO4) e vitríolo de Marte (sulfato de ferro III, Fe2(TÃO4)3).
A primeira produção de ácido sulfúrico no mundo moderno ocorreu no século XVII. O alemão Johann Glauber o obteve queimando enxofre com nitrato de potássio (KNO3). Sua fabricação formalmente reconhecida ocorreu no século 18 na Inglaterra, usando um método conhecido como “câmaras de chumbo”.
Este método consistia em lavagem de dióxido de enxofre (SO2) gás quente em vários compostos nitrogenados. Foi então dissolvido em um banho de ácido para formar o ácido da torre ou o ácido de Glover.
Este último, então, passou para uma série de câmaras de chumbo em que ele foi lavado com água, posteriormente fervido e condensado nas paredes. Foi, no entanto, uma concentração muito baixa de ácido em comparação com outros métodos atuais.
Propriedades do Ácido Sulfúrico


Propriedades físicas
- O ácido sulfúrico é um líquido oleoso e incolor com um odor particular, dependendo da sua concentração. Tem um ponto de fusão de 10 °C e um ponto de ebulição de 337 °C.
- Sua densidade é de 1,84g/cm3. É miscível (solúvel) com água, mas gera calor, dado o seu enorme efeito desidratante.
- É muito polar e conduz muito bem a corrente elétrica.
Propriedades quimicas
- É um forte oxidante.
- Reage com metais comuns, como o alumínio, formando sulfatos e bissulfatos, além de liberar hidrogênio.
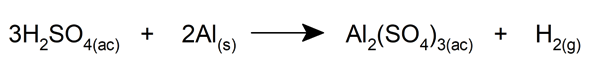

- Quando está concentrado e em altas temperaturas, reage com carbono, fósforo e enxofre. Além disso, nesta variante também pode reagir com metais preciosos.


- Decompõe sais formados por outros ácidos.
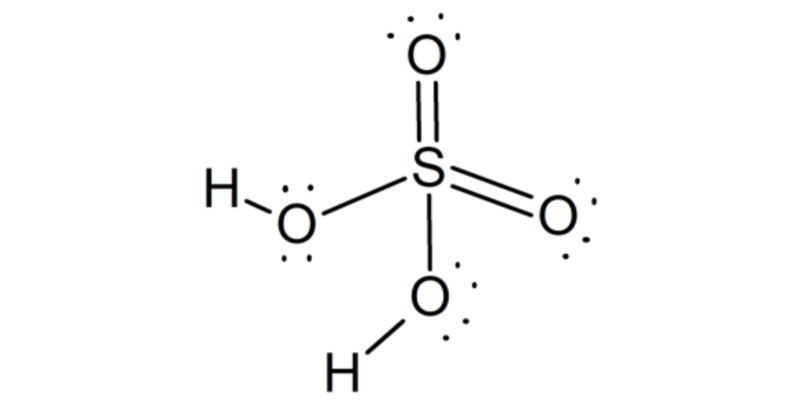
Estrutura química do ácido sulfúrico
molécula de ácido sulfúrico tem uma estrutura piramidal, com o átomo de enxofre no centro e os quatro átomos de oxigênio ligados a ele, localizados em quatro vértices. Dois dos átomos de oxigênio estão ligados ao enxofre por ligações duplas, enquanto os outros dois por ligações simples. Em duas delas, os dois átomos de hidrogênio também estão unidos.

Como é obtido o ácido sulfúrico?


Comumente, a obtenção de ácido sulfúrico Isso é feito usando os seguintes métodos:
Método de contato
Primeiro, o dióxido de enxofre (SO2) pela combustão do enxofre com oxigênio ou pela torrefação de minerais como a pirita. Depois de, dióxido de enxofre é oxidado para obter trióxido de enxofre (TÃO3).
Mais tarde, trióxido de enxofre é passado através de mecanismos de resfriamento e depois por uma torre de absorção, onde é reagido com uma amostra de ácido sulfúrico concentrado, resultando em ácido pirossulfúrico (H2S2O7)
este ácido é então decomposto por sua reação com a água, resultando em duas vezes mais ácido sulfúrico. Essa cadeia de reações é descrita a seguir:


Observe que não é aconselhável diluir o trióxido de enxofre diretamente na águapois gera uma reação exotérmica tão violenta que a maior parte do composto se volatiliza antes que possa ocorrer a formação de ácido sulfúrico.
Métodos de câmara de chumbo
ácido sulfúrico utilizado para fabricar fertilizantes É produzido principalmente por este método.
Nesse processo, dióxido de enxofre entra em altas temperaturas através do fundo de uma torre Glover (um tipo de reator químico), onde é lavado com uma solução de monóxido de nitrogênio (NO) e dióxido de nitrogênio (NO2) em ácido sulfúrico. Durante este processo, uma porção do dióxido de enxofre é oxidado a trióxido de enxofre, que é lavado com ácido para formar o ácido de Glover, um ácido que se forma na torre e é 78% H2TÃO4.
A mistura é então passada para uma câmara de chumbo, onde é tratada com água e o ácido sulfúrico se condensa nas paredes da câmara.
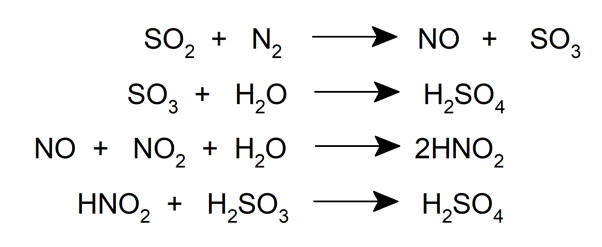
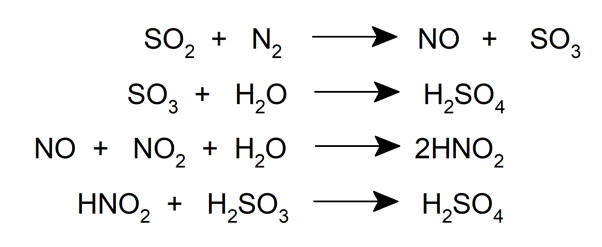
Para que serve o ácido sulfúrico?


As aplicações do ácido sulfúrico são principalmente na indústria química e petroquímica, como parte da obtenção de outros ácidos e bases. É particularmente importante na indústria de fertilizantes, bem como no refino de petróleo, processamento de aço, fabricação de explosivos, detergentes e plásticos.
Também sua importância na indústria de papel e madeira é conhecida. Também está envolvido em muitos processos na indústria têxtil e na produção de baterias. Em muitos países, sua venda está sob estrita vigilância, pois faz parte dos produtos químicos comumente usados na fabricação da cocaína.
Toxicidade do ácido sulfúrico
Torna-se claro que o ácido sulfúrico é um composto tóxico: um irritante de marca importantecapazes de corroer rapidamente a matéria orgânica, quando encontrados em altas concentrações.
Mesmo em baixa concentração, exposições repetidas podem causar dermatite ou mesmo câncer. Não há níveis seguros de inalação, ingestão ou exposição de contato para este composto.
Comercialização de ácido sulfúrico


ácido sulfúrico é o produto químico mais fabricado no mundo, e suas vendas em todo o planeta são grandes. Tanto que, em determinado momento, suas margens de produção foram utilizadas como forma de medir o grau de industrialização dos países.
O preço do quilograma pode variar de dezenas a centenas de dólares americanos, dependendo de sua concentração.
Contaminação ambiental com ácido sulfúrico
ácido sulfúrico normalmente não é encontrado na natureza e, muito menos, em altas concentrações. Portanto, constitui um composto poluente de grande impacto na vida animal e vegetal, principalmente considerando sua reação explosiva com a água.
Derramamentos do material são geralmente tratados com uma base forte (como bicarbonato) e contidos com cinzas de cimento ou outros materiais resistentes. Você nunca deve tentar diluí-lo com água.nem deve ser jogado no ralo ou esgoto.
Siga com: Ácido Acético