Explicamos o que é o magnésio, como foi descoberto e quais são as suas características. Além disso, as propriedades que possui e seus usos.

O que é magnésio?
Magnésio é um elemento químico metálicoo sétimo em abundância no planeta Terra e constituinte de íons essenciais para a vida.
É um metal leve, cor branca prateada forte médiainsolúvel e altamente reativo, por isso é comum encontrá-lo em compostos e sais.
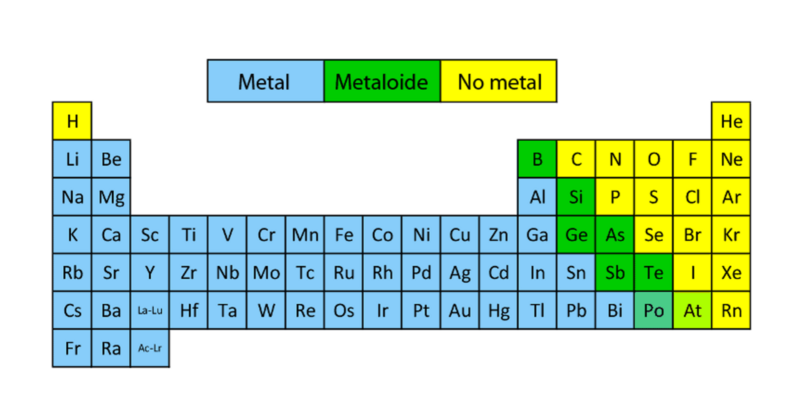
É um metal alcalino-terroso e seu comportamento químico é semelhante ao do cálcio, um elemento vizinho na tabela periódica.
magnésio está em vários alimentos, mas principalmente os de origem vegetal como sementes, nozes, ervas secas, farelo, nozes, amêndoas e muitos outros. Faz parte dos nutrientes essenciais para o corpo humano.
É representado pelo símbolo Mg.
Veja também: chumbo
descoberta do magnésio

Seu nome vem do latim magnésio e esta palavra, por sua vez, vem do grego, como a de magnetita e manganês, pois esses metais eram encontrados em abundância na Prefeitura de Magnésia, uma das quatro regiões em que se dividia a Antiga Tessália, na Grécia helênica.
magnésio foi descoberto em 1618, quando um fazendeiro inglês chamado Epsom notou que suas vacas se recusavam a beber água de um poço próximo, mas borrifá-las curava suas erupções e erupções cutâneas. Assim nasceram os sais de Epsom, que na verdade eram sulfato de magnésio hidratado (MgSO4 · 7H2QUALQUER). Seu status como elemento químico foi confirmado apenas em 1755 por Joseph Black, e sua produção como tal ocorreu em 1808 por Sir Humphry Davy.
Características atômicas do magnésio
Os átomos de magnésio têm uma valência de 2 e uma massa atômica de 24,31 u, bem como uma eletronegatividade de 1,31 na escala de Pauling. É um formador de sal frequente, porque pode facilmente formar íons positivos (Mg2+). Além disso, apresenta uma alta reatividade.
Estado natural do magnésio

É considerado que cerca de 2% da crosta terrestre é feita de magnésio e é o terceiro elemento mais abundante nas águas do mar. Porém, nunca é encontrado em seu estado metálico na natureza, mas sim como componente de compostos orgânicos e inorgânicos.
Mais de 60 minerais como a dolomita, dolomita, magnesita, brucita, carnalita e olivina têm presença abundante do elemento, que costuma ser mais facilmente obtido pela eletrólise do cloreto de magnésio, da água do mar.
Propriedades físicas do magnésio
Se trata de um metal normalmente sólidodo tipo paramagnético, com pontos de fusão e ebulição de 650 °C e 1090 °C, respectivamente.
Propriedades químicas do magnésio
Magnésio é altamente inflamável, especialmente quando em pó ou aparas, mas não em seu estado mais sólido. Isso ocorre porque geralmente é protegido do oxigênio ambiente com uma camada de óxido impermeável que é bastante difícil de remover.
Isso sim, uma vez aceso, o magnésio é difícil de extinguirpois reage com o nitrogênio do ar e gera uma chama branca muito intensa.
Papel biológico do magnésio

Magnésio é essencial para as células vivas de organismos vegetais e animaise tem uma presença abundante em clorofila e outros compostos orgânicos essenciais.
Seus íons desempenham um papel vital como parte de coenzimas e como estabilizador de DNA e RNAbem como na formação de neurotransmissores e neuromoduladores, no relaxamento muscular, vital para o músculo cardíaco, e na sua ação como energizante e calmante do corpo.
Doenças relacionadas ao magnésio
A deficiência de magnésio é muito rara, dada a sua abundância no meio ambiente e nos alimentos de uma dieta comum. No entanto, pode ocorrer como consequência de dificuldades de absorção intestinal ou do trato digestivo, ou como consequência de certos medicamentos. Os principais sintomas de sua deficiência são: irritabilidade extrema, sonolência, fadiga e fraqueza muscular.
aplicações de magnésio

As aplicações do magnésio são diversas, tanto no campo industrial (como liga metálica ou nas reações para obtenção de outros elementos, como o hidrogênio) quanto no campo médico e nutricional. Alguns de seus usos são:
- É utilizado em ligas com o alumínio, na fabricação de latas, vasilhames e autopeças.
- Seus óxidos são usados na produção de ferro e aço, vidro e cimento.
- É usado como agente redutor na obtenção de urânio.
- En hidróxidos, cloruros o sulfatos, se usa en la medicina como purgante, desinfectante o psicofármaco.
- O carbonato de magnésio é usado como dessecante em esportes para remover o suor e melhorar a aderência.
- É famosa a utilização do magnésio nas origens da fotografia (flash) e como parte de fogos de artifício e bombas incendiárias.
Isótopos
O magnésio possui vários isótopos. O mais estável é o Mg-26usado em datação radiométrica, como indicador no estudo de meteoritos e objetos de fora do sistema solar.
Precauções de Magnésio
Os principais cuidados no manuseio do magnésio tem a ver com sua extrema inflamabilidade no estado pulverizadopois reage rapidamente em contato com o calor ou o ar.
Sua extrema reatividade exige que seja separado de ácidos (produz hidrogênio abundante, também inflamável) e que uma vez aceso não tente apagar com água mas com areia seca, cloreto de sódio ou extintores de classe D.
compostos com magnésio

Alguns compostos com este elemento são:
- hidróxido de magnésio. De fórmula Mg(OH)2 É um antiácido e laxante muito comumente usado.
- Carbonato de Magnésio. Usado por atletas como dessecante, responde à fórmula MgCO3.
- Nitrato de Magnésio. De fórmula Mg(NO3)2é um sal higroscópico muito solúvel em água e etanol.